doi: 10.15389/agrobiology.2022.5.945rus
УДК 633.15:577.336
Работа выполнена при поддержке ФНТП развития сельского хозяйства РФ (подпрограмма «Аграрная наука — шаг в будущее развитие АПК»).
ОЦЕНКА ВЗАИМОСВЯЗИ ЭКСПРЕССИИ ГЕНА ЛИКОПИН-ε-ЦИКЛАЗЫ LcyE С СОДЕРЖАНИЕМ β-КАРОТИНА
И ХЛОРОФИЛЛОВ В ВЕГЕТАТИВНОЙ ТКАНИ КУКУРУЗЫ
Д.Х. АРХЕСТОВА1, 2, А.В. КУЛАКОВА1 ✉, Э.Б. ХАТЕФОВ3, А.В. ЩЕННИКОВА1, Е.З. КОЧИЕВА1
Кукуруза (Zea mays L.) — важная сельскохозяйственная культура, одним из ценных признаков которой считается биосинтез предшественников витамина А в зерне и фотосинтезирующей ткани. Количество провитамина А в зерне находится в зависимости от экспрессии гена ликопин-ε-циклазы LcyE, катализирующей образование α-каротина и участвующей в регуляции соотношения ветвей β-β и β-ε пути метаболизма каротиноидов. В настоящей работе впервые выявлено отсутствие ассоциаций между окраской зерна и содержанием суммы каротиноидов и β-каротина в листьях кукурузы, установлено наличие положительной связи между количеством β-каротина и хлорофиллов a и b, определена обратная зависимость между содержанием β-каротина и хлорофиллов a и b и уровнем экспрессии гена LycE. Целью работы был анализ корреляционной связи содержания суммы каротиноидов, β-каротина и хлорофиллов а и b с экспрессией гена LcyE в листьях инбредных линий кукурузы отечественной селекции. В работе использовали четыре инбредные линии кукурузы: три белозерные (6097-1, МБК, Тетраплоид Шумного) и одну (5580-1) с желтой окраской зерна. Зерна проращивали в увлажненной почве при 23/25 °С и режиме 16/8 ч (день/ночь) до появления 4-го настоящего листа. Суммарную РНК выделяли из 50-100 мг ткани листьев и использовали для синтеза кДНК (GoScriptтм Reverse Transcription System, «Promega», США). Экспрессию гена LcyE в листьях определяли методом количественной ПЦР в реальном времени с нормализацией данных по референсному гену Zea mays polyubiquitin (NM_001329666.1; праймеры ZmUBI-rtF: 5´-ATCGTGGTTGTGGCTTCGTTG-3´, ZmUBI-rtR: 5´-GCTGCAGAAGAGTTTTGG-GTACA-3´). Для реакции использовали 3 нг кДНК-матрицы, кДНК-специфичные праймеры (ZmLcyE-F: 5´-TTTACGTGCAAATGCAGTCAA-3´, ZmLcyE-R: 5´-TGACTCTGAAGCTAGAGAAAG-3´), набор Реакционная смесь для проведения РВ-ПЦР в присутствии SYBR GreenI и ROX (ООО «Синтол», Россия) и термоциклер CFX96 Real-Time PCR Detection System («Bio-Rad Laboratories», США). Проводили количественное определение содержания суммы каротиноидов, хлорофиллов а и b и β-каротина в листьях. Растительную ткань (0,2 г) гомогенизировали в растворе Фолча (хлороформ:метанол, 2:1 v/v) в присутствии следовых количеств Mg2CO3, инкубировали 1 ч при 4 °С в водяной бане со льдом и центрифугировали 10 мин при 4000 об/мин и 4 °С (центрифуга Eppendorf 5418 R, «Eppendorf», Германия). Собирали хлороформную фазу и измеряли содержание ликопина, β-каротина, суммы каротиноидов, хлорофиллов а и b. Спектры поглощения регистрировали на спектрофотометрах Eppendorf BioSpectrometer® basic («Eppendorf», Германия) и Cary 50 («Agilent Technology», США). Количество пигментов рассчитывали по соответствующим формулам. Корреляции между содержанием пигментов и экспрессией гена LcyE оценивали с помощью статистических методов. Самое высокое содержание каротиноидов было выявлено в листьях линии Тетраплоид Шумного. Образцы остальных трех линий синтезировали меньшее количество каротиноидов и были сходны между собой по этому параметру. В листьях линии 6097-1 было обнаружено приблизительно в 2 раза больше β-каротина и хлорофиллов a и b, чем у других анализируемых линий, несущественно различающихся между собой по количеству пигментов. Поскольку β-каротин служит предшественником ксантофиллов основного ксантофиллового цикла фотозащиты растений, можно говорить о повышенной скорости фотосинтеза в фотосинтезирующих тканях линии 6097-1 в сравнении с другими анализируемыми линиями. Соответственно, линия 6097-1 может обладать повышенной устойчивостью к оксидативному стрессу, а также служить донором признака повышенного содержания провитамина А (как силосная культура). Также установлено, что в листьях линий 5580-1 и Тетраплоид Шумного экспрессия гена LycE в ~ 4-5 раз выше, чем у линий МБК и 6097-1. Корреляционный анализ показал обратную зависимость между содержанием β-каротина и хлорофиллов a и b и уровнем экспрессии гена LycE. На основании полученных результатов мы предполагаем, что данные экспрессии гена LycE могут быть использованы в качестве экспрессионного молекулярного маркера количества провитамина А, синтезируемого в листьях кукурузы, а также при оценке степени устойчивости растения к фотоокислительному стрессу.
Ключевые слова: Zea mays L., кукуруза, ликопин-ε-циклаза, LycE, каротиноиды, хлорофиллы, экспрессия генов.
Фотосинтез сопровождается образованием в растениях активных форм кислорода (АФК), обладающих выраженной реакционной способностью (1). Действие АФК направлено на метаболические модификации белков, нуклеиновых кислот и липидов, однако избыток АФК вызывает повышенную окислительную деструкцию химических соединений в клетках.
Защита от окислительного стресса достигается за счет регуляции количества АФК и нивелирования вызываемых ими повреждений, в том числе за счет хлорофиллов и каротиноидов (2). Каротиноиды поглощают энергию света и осуществляют синглет-синглетную передачу энергии возбуждения молекулам хлорофилла. В свою очередь, хлорофиллы отдают каротиноидам избыточную энергию посредством триплет-триплетного переноса. Возвращение каротиноидов из триплетного в исходное состояние происходит благодаря рассеиванию энергии в виде тепла (1).
Следовательно, каротиноиды играют роль антиоксидантов, связанную с гашением триплетного хлорофилла и синглетного кислорода (1). Речь идет о каротиноидах ксантофиллового цикла (3), который в основном задействован в регуляции перераспределения энергии света между виолаксантином, зеаксантином и хлорофиллом а. В ответ на световой стресс виолаксантин превращается в зеаксантин через антераксантин, который действует как липидозащитный антиоксидант и стимулирует нефотохимическое тушение в светособирающем хлорофилл-a/b-белковом комплексе (3). При недостаточном освещении виолоксантин действует как светособирающее соединение, служащее для хлорофилла донором энергии. Кроме основного, у высших растений имеется дополнительный, второй, тип ксантофиллового цикла — лютеин-5,6-эпоксидный, в основе которого лежит обратимое превращение лютеина в лютеин-5,6-эпоксид (3, 4).
Биосинтез каротиноидов начинается с образования предшественника всех каротиноидов — фитоина под действием фитоинсинтазы PSY. В последующих реакциях синтезируется ликопин. Далее метаболический путь разделяется на ветви β-β и β-ε, приводящие к образованию ксантофиллов основного (зеаксантин, антераксантин, виолаксантин) и дополнительного (лютеин) типов ксантофиллового цикла. В цикле первого типа ксантофиллы представляют собой производные ветви β-β метаболического пути биосинтеза каротиноидов, когда под действием ликопин-β-циклазы (LcyB) на обоих концах линейной молекулы ликопина формируются b-иононовые кольца (β-каротин; продукты гидроксилирования β-каротина — зеаксантин, антераксантин и виолаксантин) (5, 6). В цикле второго типа ксантофиллы — это производные ветви β-ε пути биосинтеза каротиноидов. Их синтез начинается с a-каротина, который представляет собой молекулу с β-иононовым кольцом на одном конце и e-иононовым кольцом на другом конце изопреноидной цепи, образующуюся в результате совместного действия LcyB и ликопин-e-циклазы (LcyE) (конечный продукт ветви β-ε — лютеин) (5, 6).
Интересно, что β-криптоксантин (ксантофилл ветви β-β), как и α- и β-каротины, не только выполняет фотозащитную функцию в отношении растения-хозяина, но и служит предшественником дефицитного витамина А. При этом наиболее значим β-каротин, поскольку в его структуре имеется два β-иононовых кольца, вследствие чего окислительное расщепление β-каротина приводит к образованию двух молекул витамина А (7-9).
Кукуруза (Zea mays L.) играет все большую роль в экономике Российской Федерации как источник пищевого и технического зерна, а также в качестве силосной культуры. В связи с широкой направленностью использования растений кукурузы важно, чтобы предшественники витамина А содержались в повышенном количестве не только в зерне (диетическое питание), но и в фотосинтезирующей ткани (защита растения от стресса, силос с повышенной кормовой ценностью).
Силос включает надземную часть растения (початки, листья, стебли) и в кормлении сельскохозяйственных животных обеспечивает около 50 % сухого вещества основного корма (10-12). Использование фотосинтезирующей ткани (особенно листьев) растений кукурузы в животноводстве может быть более выгодно экономически в сравнении с зерном. В зерне традиционных сортов и линий кукурузы каротиноиды составляют всего 0,5-2,5 мкг/г сырой массы (13-15), тогда как ксантофиллы в листьях — около 200 мкг/г сырой массы, что примерно в 100 раз больше (16).
У кукурузы идентифицированы и охарактеризованы обе ликопин-циклазы — LycE и LycB, включая экспрессию кодирующих их генов в зерне (17-19). Однако данные об активности LycE и LycB в фотосинтезирующей ткани кукурузы отсутствуют. При этом полиморфизмы в последовательности гена LycE делают его одним из молекулярных маркеров, определяющих количество провитамина А в ткани (13, 15, 20, 21). Доноры мутантных аллелей lcyE активно используются в селекции линий кукурузы, продуцирующих обогащенное провитамином A зерно (14, 15, 22). Между экспрессией гена LycE и содержанием провитамина А существует обратная зависимость (13). Такая корреляция консервативна у высших растений, что продемонстрировано на примере листьев модельного вида Arabidopsis thaliana L. (23).
В настоящей работе впервые выявлено отсутствие ассоциаций между окраской зерна и содержанием суммы каротиноидов и β-каротина в листьях кукурузы, установлено наличие положительной связи между количеством β-каротина и хлорофиллов a и b, определена обратная зависимость между содержанием β-каротина и хлорофиллов a и b и уровнем экспрессии гена LycE. Продемонстрирована возможность использования данных по экспрессии гена LycE в листе в качестве экспрессионного молекулярного маркера количества синтезируемого в листьях провитамина А, а также степени устойчивости растения к фотоокислительному стрессу.
Целью работы был анализ корреляционной связи содержания суммы каротиноидов, β-каротина и хлорофиллов а и b с экспрессией гена LcyE в листьях инбредных линий кукурузы отечественной селекции.
Методика. В работе использовали четыре инбредные линии кукурузы: три белозерные (6097-1, МБК, Тетраплоид Шумного) и одну (5580-1) с желтой окраской зерна. Семенной материал был любезно предоставлен Институтом сельского хозяйства филиала Кабардино-Балкарского научного центра РАН (ИСХ КБНЦ РАН, КБР, Россия). Зерна проращивали в увлажненной почве при 23/25 °С и режиме 16/8 ч (день/ночь) в условиях экспериментальной установки искусственного климата ЭУИК (ФИЦ Биотехнологии РАН, Россия) до появления 4-го настоящего листа.
Суммарную РНК выделяли из 50-100 мг ткани листьев (RNeasy Plant Mini Kit, «QIAGEN», Германия), дополнительно очищали от примесей ДНК (RNase-free DNasy set, «QIAGEN», Германия) и использовали для синтеза кДНК (GoScriptтм Reverse Transcription System, «Promega», США) согласно протоколам производителей. Качество РНК проверяли методом электрофореза в 1,5 % агарозном геле. Концентрацию РНК и кДНК определяли на флуориметре Qubit 4 («Thermo Fisher Scientific», США) с помощью соответствующих реактивов (Qubit RNA HS Assay Kit и Qubit DS DNA HS Assay Kit, «Invitrogen», США).
Экспрессию гена LcyE в листьях определяли методом количественной ПЦР в реальном времени (РВ-ПЦР) с нормализацией данных по референсному гену Zea mays polyubiquitin (NM_001329666.1; праймеры ZmUBI-rtF: 5´-ATCGTGGTTGTGGCTTCGTTG-3´, ZmUBI-rtR: 5´-GCTGCAGAA-GAGTTTTGGGTACA-3´). Для реакции использовали 3 нг кДНК-матрицы, кДНК-специфичные праймеры (ZmLcyE-F: 5´-TTTACGTGCAAATGCAG-TCAA-3´, ZmLcyE-R: 5´-TGACTCTGAAGCTAGAGAAAG-3´), набор Реакционная смесь для проведения РВ-ПЦР в присутствии SYBR GreenI и ROX (ООО «Синтол», Россия) и термоциклер CFX96 Real-Time PCR Detection System («Bio-Rad Laboratories», США). Реакции проводили в трех технических и двух биологических повторах. Программа для РВ-ПЦР была следующей: 5 мин при 95 °С (исходная денатурация); 15 с при 95 °С (денатурация), 40 с при 60 °С (отжиг и синтез) (40 циклов).
Количественное определение содержания (мг/г сырой массы) суммы каротиноидов, хлорофиллов а и b и β-каротина в листьях проводили в трех технических и двух биологических повторах (24-26). Растительную ткань (0,2 г) гомогенизировали в растворе Фолча (хлороформ:метанол, 2:1 v/v) в присутствии следовых количеств Mg2CO3, инкубировали 1 ч при 4 °С в водяной бане со льдом и центрифугировали 10 мин при 4000 об/мин и 4 °С (центрифуга Eppendorf 5418 R, «Eppendorf», Германия). Собирали хлороформную фазу и измеряли содержание ликопина, β-каротина, суммы каротиноидов, хлорофиллов а и b. Спектры поглощения регистрировали на спектрофотометрах Eppendorf BioSpectrometer® basic («Eppendorf», Германия) и Cary 50 («Agilent Technology», США). Количество пигментов рассчитывали по соответствующим формулам (24, 25).
Полученные результаты обрабатывали с помощью GraphPad Prism v.8 («GraphPad Software Inc.», США; https://www.graphpad.com/scientific-software/prism/). Данные выражали как средние значения (M) со стандартными отклонениями (±SD). Для оценки достоверности различий в экспрессии гена или в содержании пигментов между линиями кукурузы использовали t-критерий Уэлча (unequal variance, Welch’s t-test) (при р < 0,05 различия статистически значимы). Корреляции между содержанием пигментов и экспрессией гена LcyE в листьях линий кукурузы также оценивали с помощью GraphPad Prism v.8. Корреляция однозначно присутствовала при R2 > 0,7, была высоковероятна при R2 = 0,4-0,7 и отсутствовала при R2 < 0,4.
Результаты. Разные оттенки окраски зерна кукурузы (от желтого до оранжевого) зависят от состава и количественного соотношения каротиноидов (27). Поэтому белозерные линии 6097-1, МБК и Тетраплоид Шумного были взяты в качестве образцов с предположительно нарушенным синтезом цветных каротиноидов (ликопина, каротинов, ксантофиллов). Желтозерная линия 5580-1 с сохраненным биосинтезом цветных каротиноидов служила контролем. Мы также определяли возможные соответствия между особенностями биосинтеза каротиноидов в зерне и фотосинтезирующей ткани. Темно-зеленая окраска листьев у всех четырех анализируемых линий свидетельствовала об успешном фотосинтезе и фотозащите, то есть в листьях осуществлялся биосинтез ксантофиллов (3).
Наибольшее содержание каротиноидов в листьях наблюдалось у линии Тетраплоид Шумного (рис. 1, А). Остальные линии синтезировали меньшее количество каротиноидов и были схожи между собой по этому показателю. В листьях линии 6097-1 было приблизительно в 2 раза больше β-каротина, чем у других анализируемых образцов (см. рис. 1, Б). В случае хлорофиллов а и b наблюдался сходный с β-каротином количественный профиль (см. рис. 1, В, Г).
Таким образом, было подтверждено отсутствие ассоциаций между окраской зерна и содержанием суммы каротиноидов и β-каротина в листьях кукурузы. Мы предполагаем, что это может быть связано с активностью других генов пути биосинтеза каротиноидов, например гена фитоинсинтазы PSY, которая катализирует синтез предшественника всех каротиноидов — фитоина. Геном кукурузы содержит три паралога PSY: синтез каротиноидов в эндосперме зерна запускает PSY1, тогда как каротиногенез в листьях зависит прежде всего от активности PSY2 (16).
Данные анализа позволяют также предположить наличие положительной связи между количеством β-каротина и хлорофиллов а и b. Поскольку β-каротин служит предшественником ксантофиллов основного ксантофиллового цикла фотозащиты растений (3), можно говорить о повышенной скорости фотосинтеза в фотосинтезирующих тканях линии 6097-1 в сравнении с другими анализируемыми линиями. Соответственно, линия 6097-1 может обладать повышенной устойчивостью к оксидативному стрессу, а также быть донором признака повышенного содержания провитамина А как силосная культура.
Известно, что тип каротинов и ксантофиллов определяется соотношением ветвей β-ε и β-β пути биосинтеза каротиноидов, зависящим от уровней экспрессии генов LcyE и ликопин-β-циклазы LcyB. Кроме того, на накопление β-каротина влияет активность гена β-каротингидроксилазы 1 (β-CH, или crtRB1) (28).
В тех же тканях листа мы определили экспрессию гена ликопин-e-циклазы LycE (рис. 2). Экспрессия оказалась наибольшей в листьях у линии 5580-1 и немного ниже — у линии Тетраплоид Шумного. В листьях линий МБК и 6097-1 транскрипция гена была в ~ 4-5 раз ниже (см. рис. 2). Такой межобразцовый профиль соответствует показанной ранее обратной зависимости между экспрессией LycEи содержанием провитамина А (13, 22). Высокая экспрессия LycE предположительно означает смещение биосинтеза каротиноидов в сторону ветви β-ε с наработкой a-каротина и ксантофиллов неосновного (второго) типа ксантофиллового цикла с образованием лютеина и его производных.
Корреляционный анализ подтвердил наши предположения. В то время как не наблюдалось зависимости между уровнем экспрессии гена LycE и содержанием суммы каротиноидов (рис. 3, А), обратная корреляция между экспрессией гена LycE и количеством β-каротина, хлорофиллов а и b (см. рис. 3, Б-Г) была предсказана с высокой вероятностью. Это согласуется с ранее полученными данными для фотосинтезирующей ткани A. thaliana (23).
Таким образом, окраска зерна кукурузы не коррелирует с содержанием суммы каротиноидов и β-каротина в листьях. При этом в листьях обнаружена положительная связь между количествами β-каротина и хлорофиллов a и b. Кроме того, показана обратная зависимость между содержанием β-каротина и хлорофиллов a и b и уровнем экспрессии гена LycE. На основании полученных результатов мы предполагаем, что данные по экспрессии гена LycE могут быть использованы в качестве экспрессионного молекулярного маркера количества провитамина А, синтезируемого в листьях кукурузы, а также при оценке степени устойчивости растения к фотоокислительному стрессу.
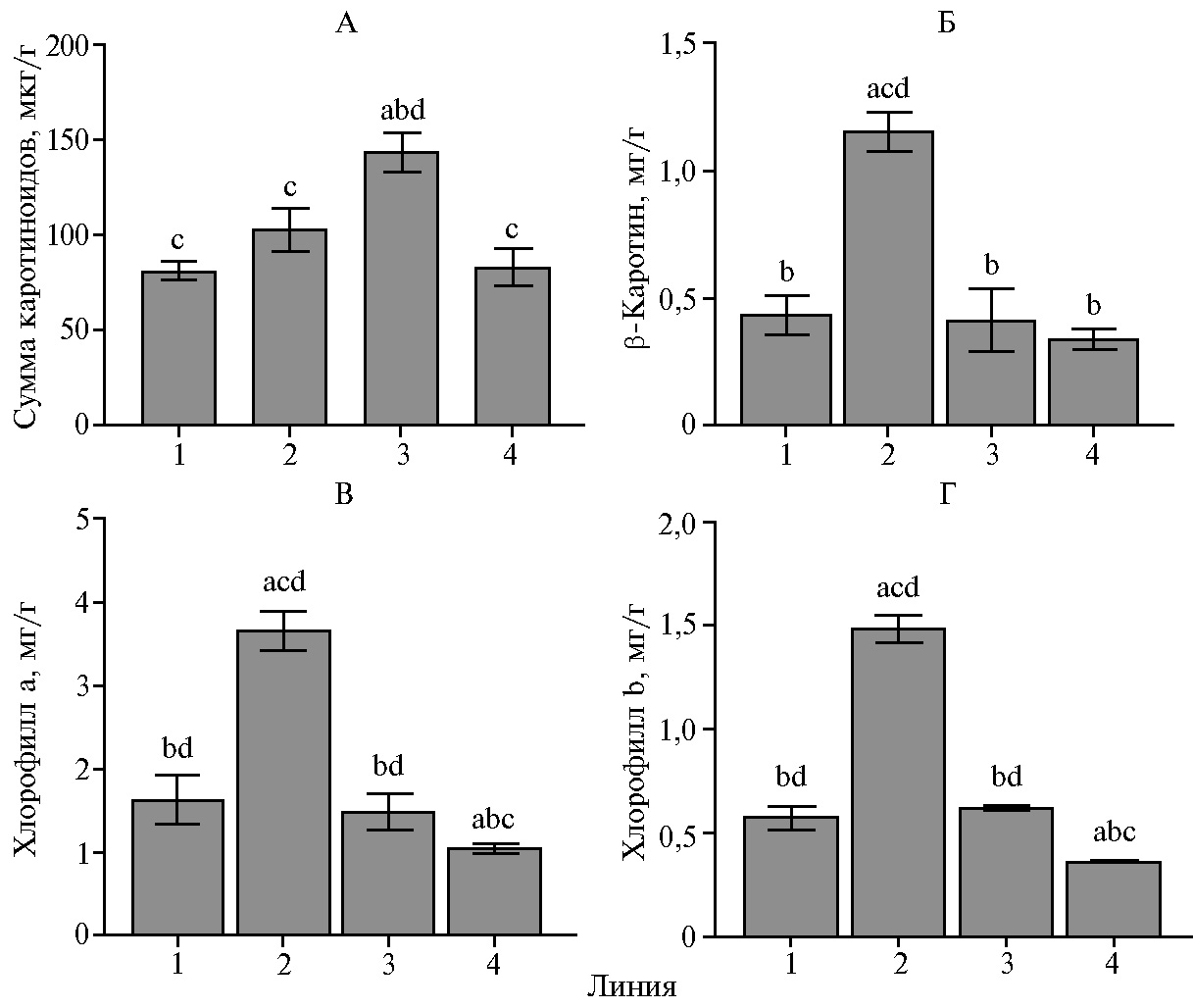
Рис. 1. Содержание суммы каротиноидов (А), b-каротина (Б), хлорофилла а (В) и хлорофилла b (Г) в листьях инбредных линий кукурузы (Zea mays L.): 1 — МБК, 2 — 6097-1, 3 — Тетраплоид Шумного, 4 — 5580-1 (лабораторный опыт, n = 3, N = 2).
a, b, c, d Различия между образцами статистически значимы при p < 0,001.
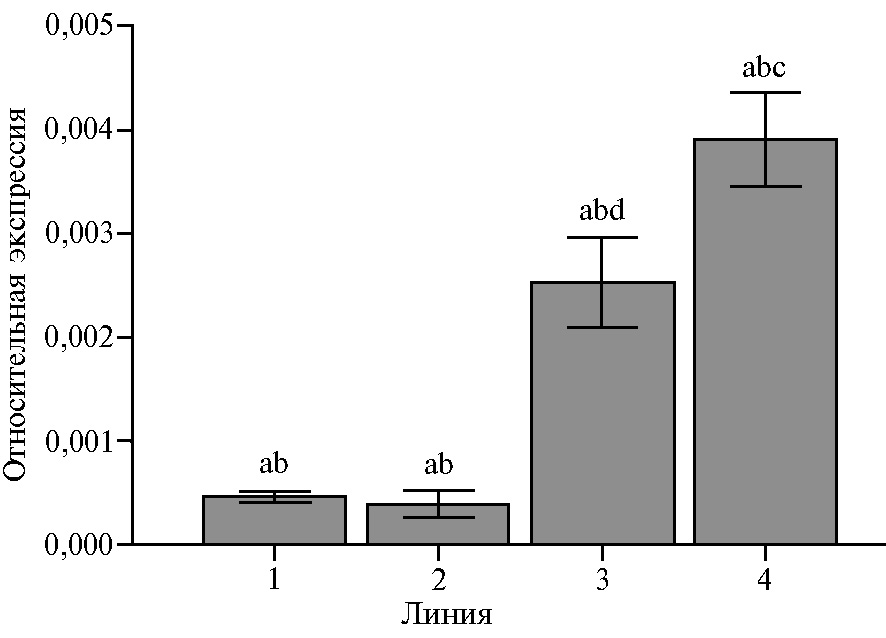
Рис. 2. Относительная экспрессия гена LcyE в листьях инбредных линий кукурузы (Zea mays L.): 1 — МБК, 2 — 6097-1, 3 — Тетраплоид Шумного, 4 — 5580-1 (лабораторный опыт, n = 3, N = 2). a, b, c, d Различия между образцами статистически значимы при p < 0,001.
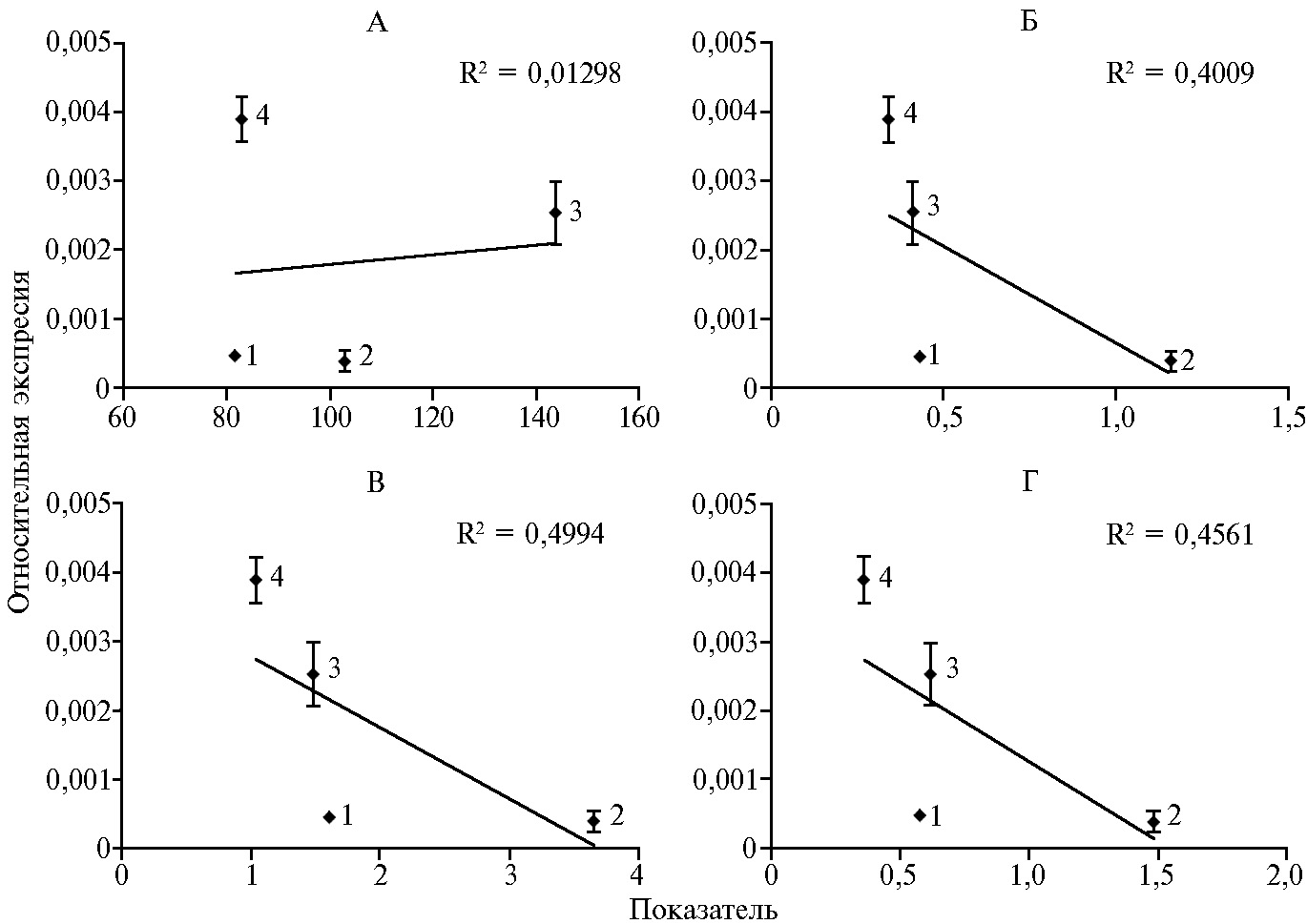
Рис. 3. Оценка корреляции между относительной экспрессией гена LcyE и содержанием суммы каротиноидов (мкг/г) (А), β-каротина (мг/г) (Б), хлорофилла а (мг/г) (В) и хлорофилла b (мг/г) (Г) в листьях инбредных линий кукурузы (Zea mays L.): 1 — МБК, 2 — 6097-1, 3 — Тетраплоид Шумного, 4 — 5580-1 (лабораторный опыт, n = 3, N = 2).
ЛИТЕРАТУРА
- Maoka T. Carotenoids as natural functional pigments. Journal of Natural Medicines, 2020, 74(1): 1-16 (doi: 10.1007/s11418-019-01364-x).
- Baroli I., Niyogi K.K. Molecular genetics of xanthophyll-dependent photoprotection in green algae and plants. Philosophical Transactions of The Royal Society B Biological Sciences, 2000, 355(1402): 1385-1394 (doi: 10.1098/rstb.2000.0700).
- Jahns P., Holzwarth A.R. The role of the xanthophyll cycle and of lutein in photoprotection of photosystem II. Biochimica et Biophysica Acta (BBA) - Bioenergetics, 2012, 1817(1): 182-193 (doi: 10.1016/j.bbabio.2011.04.012).
- Ладыгин В.Г. Лютеин-5,6-эпоксидный цикл — новый ксантофилловый цикл в хлоропластах растений. Биологические мембраны, 2008, 25(3): 163-172.
- Cunningham F.X. Jr, Pogson B., Sun Z., McDonald K.A., DellaPenna D., Gantt E. Functional analysis of the β and e lycopene cyclase enzymes of Arabidopsis reveals a mechanism for control of cyclic carotenoid formation. Plant Cell, 1996, 8: 1613-1626 (doi: 10.1105/tpc.8.9.1613).
- Rosas-Saavedra C., Stange C. Biosynthesis of carotenoids in plants: enzymes and color. In: Carotenoids in nature. Subcellular biochemistry, vol. 79 /C. Stange (ed.). Springer, Cham, 2016: 35-69 (doi: 10.1007/978-3-319-39126-7_2).
- Wong J.C., Lambert R.J., Wurtzel E.T., Rocheford T.R. QTL and candidate genes phytoene synthase and zeta-carotene desaturase associated with the accumulation of carotenoids in maize. Theoretical and Applied Genetics, 2004, 108(2): 349-359 (doi: 10.1007/s00122-003-1436-4).
- Krinsky N.I., Johnson E.J. Carotenoid actions and their relation to health and disease. Molecular Aspects of Medicine, 2005, 26(6): 459-516 (doi: 10.1016/j.mam.2005.10.001).
- Nagao A., Olson J.A. Enzymatic formation of 9-cis, 13-cis, and all-trans retinals from isomers of beta-carotene. The FASEB Journal, 1994, 8(12): 968-973 (doi: 10.1096/fasebj.8.12.8088462).
- Cabiddu A., Delgadillo-Puga C., Decandia M., Molle A.G. Extensive ruminant production systems and milk quality with emphasis on unsaturated fatty acids, volatile compounds, antioxidant protection degree and phenol content. Animals, 2019, 9(10): 771 (doi: 10.3390/ani9100771).
- Graulet B., Cirié C., Martin B. Contrasted effects of dietary extruded linseed supplementation on carotenoid and liposoluble vitamin status in lactating Holstein or Montbéliarde cows fed hay or corn silage. Journal of Dairy Science, 2019, 102(7): 6210-6225 (doi: 10.3168/jds.2018-16138).
- Mitani T., Kobayashi K., Ueda K., Kondo S. Regional differences in the fatty acid composition, and vitamin and carotenoid concentrations in farm bulk milk in Hokkaido, Japan. Journal of Animal Science, 2021, 92(1): e13570 (doi: 10.1111/asj.13570).
- Harjes C.E., Rocheford T.R., Bai L., Brutnell T.P., Kandianis C.B., Sowinski S.G., Stapleton A.E., Vallabhaneni R., Williams M., Wurtzel E.T., Yan J., Buckler E.S. Natural genetic variation in lycopene epsilon cyclase tapped for maize biofortification. Science, 2008, 319(5861): 330-333 (doi: 10.1126/science.1150255).
- Yadav O.P., Hossain F., Karjagi C.G., Kumar B., Zaidi P.H., Jat S.L., Chawla J.S., Kaul J., Hooda K.S., Kumar P., Yadava P., Dhillon B.S. Genetic improvement of maize in India: retrospect and prospects. Agricultural Research, 2015, 4(4): 325-338 (doi: 10.1007/s40003-015-0180-8).
- Zunjare R.U., Chhabra R., Hossain F., Baveja A., Muthusamy V., Gupta H.S. Molecular characterization of 5' UTR of the lycopene epsilon cyclase (lcyE) gene among exotic and indigenous inbreds for its utilization in maize biofortification. 3 Biotech, 2018, 8(1): 75 (doi: 10.1007/s13205-018-1100-y).
- Li F., Vallabhaneni R., Yu J., Rocheford T., Wurtzel E.T. The maize phytoene synthase gene family: overlapping roles for carotenogenesis in endosperm, photomorphogenesis, and thermal stress tolerance. Plant Physiology, 2008, 147(3): 1334-1346 (doi: 10.1104/pp.108.122119).
- Bai L., Kim E.-H., DellaPenna D., Brutnell T.P. Novel lycopene epsilon cyclase activities in maize revealed through perturbation of carotenoid biosynthesis. Plant Journal, 2009, 59(4): 588-599 (doi: 10.1111/j.1365-313X.2009.03899.x).
- Luo H., He W., Li D., Bao Y., Riaz A., Xiao Y., Song J., Liu C. Effect of methyl jasmonate on carotenoids biosynthesis in germinated maize kernels. Food Chemistry, 2020, 307: 125525 (doi: 10.1016/j.foodchem.2019.125525).
- He W., Wang Y., Dai Z., Liu C., Xiao Y., Wei Q., Song J., Li D. Effect of UV-B radiation and a supplement of CaCl2 on carotenoid biosynthesis in germinated corn kernels. Food Chemistry, 2019, 278: 509-514 (doi: 10.1016/j.foodchem.2018.11.089).
- Zunjare R.U., Hossain F., Muthusamy V., Baveja A., Chauhan H.S., Bhat J.S., Thirunavukkarasu N., Saha S., Gupta H.S. Development of biofortified maize hybrids through marker-assisted stacking of β-carotene hydroxylase, lycopene-e-cyclase and opaque2 genes. Frontiers in Plant Sciences, 2018, 9: 178 (doi: 10.3389/fpls.2018.00178).
- Baveja A., Muthusamy V., Panda K.K., Zunjare R.U., Das A.K., Chhabra R., Mishra S.J., Mehta B.K., Saha S., Hossain F. Development of multinutrient-rich biofortified sweet corn hybrids through genomics-assisted selection of shrunkeN2, opaque2, lcyE and crtRB1 genes. Journal of Applied Genetics, 2021, 62(3): 419-429 (doi: 10.1007/s13353-021-00633-4).
- Babu R., Rojas N.P., Gao S., Yan J., Pixley K. Validation of the effects of molecular marker polymorphisms in LcyE and CrtRB1 on provitamin A concentrations for 26 tropical maize populations. Theoretical and Applied Genetics, 2013, 126(2): 389-399 (doi: 10.1007/s00122-012-1987-3).
- Pogson B.J., Rissler H.M. Genetic manipulation of carotenoid biosynthesis and photoprotection. Philosophical Transactions of The Royal Society B Biological Sciences, 2000, 355(1402): 1395-1403 (doi: 10.1098/rstb.2000.0701).
- Lichtenthaler H.K., Buschmann C. Chlorophylls and carotenoids: measurement and characterization by UV-VIS spectroscopy. Current Protocols in Food Analytical Chemistry, 2001: F4.3.1-F4.3.8 (doi: 10.1002/0471142913.faf0403s01).
- Efremov G.I., Slugina M.A., Shchennikova A.V., Kochieva E.Z. Dierential regulation of phytoene synthase PSY1 during fruit carotenogenesis in cultivated and wild tomato species (Solanum section Lycopersicon). Plants, 2020, 9(9): 1169 (doi: 10.3390/plants9091169).
- Филюшин М.А., Джос Е.А., Щенникова А.В., Кочиева Е.З. Зависимость окраски плодов перца от соотношения основных пигментов и профиля экспрессии генов биосинтеза каротиноидов и антоцианов. Физиология растений, 2020, 67(6): 644 (doi: 10.31857/S0015330320050048).
- Owens B.F., Mathew D., Diepenbrock C.H., Tiede T., Wu D., Mateos-Hernandez M., Gore M.A., Rocheford T. Genome-wide association study and pathway-level analysis of kernel color in maize. G3 Genes|Genomes|Genetics, 2019, 9(6): 1945-1955 (doi: 10.1534/g3.119.400040).
- Mehta B.K., Chhabra R., Muthusamy V., Zunjare R.U., Baveja A., Chauhan H.S., Prakash N.R., Chalam V.C., Singh A.K., Hossain F. Expression analysis of β-carotene hydroxylase1 and opaque2 genes governing accumulation of provitamin-A, lysine and tryptophan during kernel development in biofortified sweet corn. 3 Biotech, 2021, 11(7): 325 (doi: 10.1007/s13205-021-02837-1).