УДК 636/639:614.31
МЕТОДЫ САНИТАРНОГО КОНТРОЛЯ ЖИВОТНОВОДЧЕСКОЙ ПРОДУКЦИИ. СООБЩЕНИЕ IV. ИММУНОФЕРМЕНТНЫЙ АНАЛИЗ ЦИПРОФЛОКСАЦИНА И ЕГО АНАЛОГОВ
А.А. БУРКИН1, Г.П. КОНОНЕНКО1, М.А. БУРКИН2
На основе поликлональных кроличьих антител к конъюгату ципрофлоксацина с бычьим сывороточным альбумином, полученному в условиях карбодиимидной конденсации, разработан метод непрямого конкурентного иммуноферментного анализа противомикробных веществ группы фторхинолонов. С иммобилизованными конъюгатами, гетерологичными иммуногену по белковому носителю (желатин) или по методу синтеза (реакция с активированным N-гидроксисукцин-имидным эфиром и формальдегидная конденсация), чувствительность определения ципрофлоксацина и энрофлоксацина составила 0,1 нг/мл, норфлоксацина и пефлоксацина — 0,4 нг/мл. Обсуждается возможность применения иммуноферментных тест-систем для контроля остатков этих веществ в молоке, мясе и яйцах.
Ключевые слова: ципрофлоксацин, энрофлоксацин, норфлоксацин, пефлоксацин, иммуноанализ, молоко, мясо, яйца.
Современные синтетические противомикробные средства — фторхинолоны широко используются в различных отраслях животноводства в составе ветеринарных препаратов. Чаще всего они представлены N1-цик-лопропил-3-карбокси-6-фтор-7-пиперазинилхинолонами — ципрофлоксацином (ЦФ, R = H) и энрофлоксацином (ЭФ, R = CH2CH3) (формула слева), а также их N1-этилзамещенными аналогами норфлоксацином (НФ, R = H) и пефлоксацином (ПФ, R = CH3) (формула справа):

Регламенты по суммарному содержанию остаточных количеств ЦФ и ЭФ в мясной, молочной и рыбной продукции действуют в ЕС уже два десятилетия (1). За рубежом попытки разработать методы иммуноанализа для их индикации были предприняты в 1998-2006 годах (2-5), и в настоящее время там расширяется коммерческий выпуск аналитических тест-сис-тем для контроля молока, мяса, рыбы и креветок.
Целью работы стало получение иммунореагентов и оптимизация условий непрямого конкурентного иммуноферментного анализа (ИФА) на основе ципрофлоксацина, удовлетворяющего по специфичности и чувствительности нормативам на остаточное содержание фторхинолонов в животноводческой продукции.
Методика. В работе использовали N-гидроксисукцинимид (ГСИ), 1-этил-3(3-диметиламинопропил)карбодиимид (КДИ), формальдегид, диметилформамид (ДМФА), о-фенилендиамин, пероксидазу хрена (КФ 1.11.1.7) («Sigma», США), антисыворотку осла к иммуноглобулинам кролика, бычий сывороточный альбумин (БСА), яичный альбумин (ЯА) и желатин (Жел) отечественного производства.
Все вещества группы фторхинолонов получали из фармацевтических препаратов. К тщательно измельченным таблеткам РеЦипро 250 («Aurobindo Farma Ltd.», Индия), содержащего моногидрат гидрохлорида ЦФ, добавляли метанол, интенсивно смешивали, оставляли на 1 сут, затем фильтровали, высушивали фильтрат в вакууме при 40 °С и остаток взвешивали. Для подтверждения идентичности вещества снимали УФ-спек-тры. Чистоту продукта оценивали, сравнивая его концентрацию в растворе, определенную весовым методом и спектрофотометрически, после чего использовали в реакциях конъюгирования с белками. Для извлечения ЭФ, НФ и ПФ к лекарственным формам (порошок или таблетки) препаратов Энроксил («KRKA», Словения), Нолицин («KRKA», Словения) и Абактал («Lek», Словения) добавляли ДМФА в объеме, соответствующем количеству каждой субстанции (мл/мг), интенсивно смешивали, оставляли на 1 сут и фильтровали. Аликвоты фильтратов разбавляли водой, после измерения концентрации методом УФ-спектрометрии полученные растворы использовали для оценки перекрестной реактивности антител. Калибровочные растворы ЦФ для анализа готовили на основе препарата Ципрофлоксацин инъекционный («Wockhardt Ltd.», Индия) с учетом номинального значения эквивалентов ЦФ.
Для синтеза конъюгатов БСА-ЦФа (со 100-кратным мольным избытком гаптена) и Жел-ЦФа (с 25-кратным мольным избытком гаптена) в реакции активированных ГСИ-эфиров навески ГСИ (2 мг, 17 мкмоль) и КДИ (3,3 мг, 17 мкмоль) добавляли к 1,08 мл раствора ЦФ (4 мг, 12,1 мкмоль) в ДМФА. Через 24 ч перемешивания при комнатной температуре по каплям 0,89 мл реакционной смеси добавляли к БСА (7 мг, 0,1 мкмоль) и 0,11 мл — к Жел (8 мг, 0,05 мкмоль), растворенным в 2 мл 0,05 М карбонат-бикарбонатного буфера (рН 9,5), перемешивали при комнатной температуре 2 ч и диализовали. При получении конъюгатов БСА-ЦФк (со 170-кратным мольным избытком гаптена) и ЯА-ЦФк (с 60-кратным мольным избытком гаптена) в условиях карбодиимидной конденсации к растворам БСА (5 мг, 0,07 мкмоль) и ЯА (4 мг, 0,1 мкмоль) в 2 мл воды добавляли ЦФ (соответственно 4 и 2 мг, или 12 и 6 мкмоль) и КДИ (30 и 25 мг, 156 и 130 мкмоль). Реакционные смеси оставляли на 4 ч для перемешивания при 30 °С, затем еще на 20 ч при 4 °С и диализовали. Синтез БСА-ЦФф (со 100-кратным мольным избытком гаптена) в реакции формальдегидной конденсации осуществляли, добавляя к раствору БСА (5 мг, 0,07 мкмоль) в 1,5 мл воды ЦФ (7 мкмоль) и 0,3 мл 37 % раствора формальдегида (3690 мкмоль), смесь перемешивали при 30 °С 3 ч и диализовали. Для диализа использовали три смены 1000-кратных объемов 0,5 % NaCl в течение 2 сут. К продуктам диализа добавляли равный объем глицерина до концентрации 1 мг/мл (по белку) и хранили при -10 °С.
Процедуры иммунизации и конкурентного ИФА не отличались от описанных ранее (6). За развитием иммунного ответа у животных следили, анализируя взаимодействие сыворотки от каждого отбора крови с иммобилизованным конъюгатом БСА-ЦФф. После стабилизации титров антител сыворотки тестировали с другими иммобилизованными конъюгатами на связывание и торможение в конкурентном анализе с ЦФ. Твердофазные антигены, для которых верхняя граница линейного участка калибровочного графика соответствовала самым низким значениям концентрации свободного ЦФ, далее использовали для оценки перекрестной реактивности антител в отношении ЭФ, НФ и ПФ. Перекрестную реактивность антител определяли как отношение концентрации раствора ЦФ, вызывающей 50 % ингибирование связывания с твердой фазой (ИК50), к соответствующим концентрациям других свободных фторхинолонов, выраженное в процентах. УФ-спектры записывали на приборе Hitachi-557 (Япония). ИФА выполняли на микропланшетах Dynatech с регистрацией результатов на фотометре Dynatech MR5000 (Германия).
С помощью оптимизированного варианта тест-системы анализировали пробы коровьего молока, мяса кур, куриных субпродуктов и яиц из торговой сети г. Москвы. Подготовка проб для анализа не отличалась от описанной ранее (7). Молоко разбавляли фосфатно-солевым буфером (рН 7,5), состоящим из 0,01 М Na2HPO4, 0,14 M NaCl и 0,05 % Твина 20 (ФСБ-т). Гомогенаты мясной продукции и яиц взвешивали, высушивали на алюминиевых подложках с помощью термовентилятора, экстрагировали смесью ацетонитрила и воды в объемном соотношении 84:16 в течение 14 ч с интенсивным перемешиванием в начале и конце экстракции; экстракты разбавляли в 10 раз ФСБ-т.
Результаты. Подтверждение номинального значения эквивалентов ЦФ в готовой форме препарата («Wockhardt Ltd.», Индия) было получено
| 1. Характеристики УФ-поглощения приготовленных водных растворов фторхинолонов | |||
Вещество |
Расположение максимумов |
Соотношение интенсивности |
|
λ1, λ2, λ3, нм |
А1/А2 |
А2/А3 |
|
ЦФ (8) |
275, 318, 328 |
3,0 |
1,06 |
ЭФ |
272, 321, 330 |
2,7 |
1,03 |
НФ |
273, 320, 330 |
2,8 |
1,05 |
ПФ |
273, 320, 330 |
3,0 |
1,05 |
П р и м е ч а н и е. ЦФ, ЭФ, НФ и ПФ — соответственно ципрофлоксацин, энрофлоксацин, норфлоксацин, пефлоксацин. |
|||
|
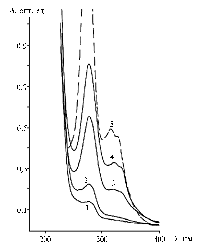
Рис. 1. Спектры УФ-поглощения бычьего сывороточного альбумина (БСА) (1), конъюгатов БСА-ЦФа (2), БСА-ЦФк (3), БСА-ЦФф (4) и ципрофлоксацина (ЦФ) (5). ЦФа, ЦФк, ЦФф — ЦФ, присоединенный к белку соответственно в реакции активированных эфиров, карбодиимидной конденсации и формальдегидной конденсации. |
при сопоставлении удельного показателя поглощения (А, 1 %, 1 см) при λ = 275 нм для раствора, приготовленного его 200-крат-ным разбавлением водой, и соответствующей величины, приведенной И.В. Титовым с соавт. (8).
В водных растворах гидрохлорида ЦФ, полученного из таблетированной формы препарата, расположение максимумов УФ-поглощения и соотношение их интенсивности совпадали с установленными для эталонных образцов (табл. 1). Для ЭФ, НФ и ПФ эти показатели были практически идентичными и незначительно отличались от свойственных ЦФ.
По полному УФ-спектру ЦФ (8) рассчитывали молярные экстинкции для максимумов поглощения при λ = 275 нм (ε = 37480), λ = 318 нм (ε = 12490) и λ = 328 нм (ε = 11760), которые далее были использованы для уточнения концентраций аналитических растворов фторхинолонов. Поль-зуясь этими же значениями, получали подтверждение достаточной степени чистоты сухого образца ЦФ, предназначенного для конъюгирования с белками. По результатам спектральных измерений его раствор с концентрацией 1 мг/мл, определенной весовым методом, после 100-кратного разбавления водой имел концентрацию 11,6±0,3 мкг/мл.
Факт образования конъюгатов ЦФ с БСА в трех различных реакциях конденсации был четко подтвержден спектральным анализом (см. рис. 1). Наряду с усилением поглощения при λ = 280 нм в спектрах продуктов реакций появился новый пик при λ = 325-328 нм, свойственный гаптену. По сравнению с карбодиимидной конденсацией реакция активированного N-гидроксисукцинимидного эфира в условиях 24-часового взаимодействия имела меньший выход (эпитопная плотность полученного конъюгата была ниже). При формальдегидной конденсации со 100-кратным мольным избытком нагрузка оказалась еще слабее. В двух последних из использованных реакций затруднения могли быть вызваны стерическими препятствиями, поскольку в них вовлекались структуры базовой части молекулы гаптена, а не удаленные от нее функциональные группы.
 |
Рис. 2. Степень связывания антител к БСА-ЦФа, полученных при 1-5-м отборах крови (1-5), с твердофазным антигеном БСА-ЦФф в концентрации 0,05 мкг/мл в присутствии ЦФ (сокращенные обозначения см. на рисунке 1). |
В качестве иммуногенов были использованы конъюгаты БСА-ЦФа и БСА-ЦФк. Первая же антисыворотка к БСА-ЦФа в условиях взаимодействия с твердофазным БСА-ЦФф позволила выявлять ЦФ вплоть до концентрации 10 нг/мл, в дальнейшем чувствительность определения возросла на порядок, а после 5-го отбора крови оказалось возможным определять менее 1 нг/мл (рис. 2).
Со всеми иммобилизованными антигенами антитела узнавали преимущественно ЦФ (табл. 2). С антигеном Жел-ЦФа, гомологичным иммуногену по методу синтеза, имела место достаточно высокая перекрестная реактивность с тремя ближайшими аналогами ЦФ, которая снижалась по мере возрастания структурных различий: для ЭФ, НФ и ПФ соответственно 68; 41 и 24 %.
| 2. Перекрестная реактивность антител к БСА-ЦФа в отношении фторхинолонов при взаимодействии с различными иммобилизованными антигенами | ||||||
Свободный антиген |
Иммобилизованный антиген (С = 0,05 мкг/мл) |
|||||
Жел-ЦФа |
ЯА-ЦФк |
БСА-ЦФф |
||||
% |
ИК50, нг/мл |
% |
ИК50, нг/мл |
% |
ИК50, нг/мл |
|
ЦФ |
100 |
5,9 |
100 |
2,0 |
100 |
0,9 |
ЭФ |
68 |
8,7 |
23 |
8,8 |
31 |
2,9 |
НФ |
41 |
14,5 |
21 |
9,6 |
8 |
17,0 |
ПФ |
24 |
24,6 |
14 |
14,5 |
6 |
14,0 |
П р и м е ч а н и е. ЦФ, ЭФ, НФ и ПФ — соответственно ципрофлоксацин, энрофлоксацин, норфлоксацин, пефлоксацин; БСА, Жел, ЯА — бычий сывороточный альбумин, желатин, яичный альбумин; ЦФа, ЦФк, ЦФф — ЦФ, присоединенный к соответствующему белку в реакции активированных эфиров, карбодиимидной конденсации и формальдегидной конденсации. |
||||||
Интересно отметить, что аналогичные свойства имела и ранее описанная аналитическая система на основе антител к БСА-ЦФа и иммобилизованного конъюгата ЦФ с человеческим сывороточным альбумином, в которой относительная конкурентная способность ЭФ составила 69,8 %, НФ — 44,6 % (3).
Иммобилизация конъюгата ЯА-ЦФк, синтезированного КДИ-кон-денсацией, мало повлияла на специфичность анализа, произошло лишь некоторое снижение узнавания тех же трех соединений по сравнению с ЦФ. В отношении продукта формальдегидной конденсации ЦФ и БСА ана-
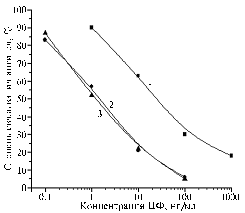 |
Рис. 3. Степень связывания антител к БСА-ЦФк, полученных при 1-3-м отборах крови (1-3), с твердофазным антигеном БСА-ЦФф в концентрации 0,15 мкг/мл в присутствии ЦФ (сокращенные обозначения см. на рисунке 1). |
литические возможности антител к БСА-ЦФа изменялись. Выраженное узнавание сохранялось только для ЭФ (31 %), с другими веществами перекрестная реактивность составила всего 6-8 %. Иммобилизация БСА-ЦФф обеспечивала наибольшую чувствительность анализа, что можно объяснить его явной гетерологичностью по отношению к иммуногену из-за иного участка связывания молекулы (вероятнее всего, по протонам ароматического ядра).
Развитие иммунного ответа на введение БСА-ЦФк было также выраженным, и во 2-й и 3-й сыворотках антитела с рабочим титром 1:25 000 обеспечивали в кон-курентном анализе с гетерологичным твердофазным БСА-ЦФф уверенное определение ЦФ вплоть до 0,1 нг/мл (рис. 3). При предварительном тестировании антител с гомологичным ЯА-ЦФк была выявлена чрезвычайно высокая степень связывания при отсутствии торможения ЦФ даже в концентрации 1000 нг/мл, поэтому последующая оценка указанной антисыворотки проводилась только с двумя твердофазными антигенами (табл. 3).
| 3. Перекрестная реактивность антител к БСА-ЦФк в отношении фторхинолонов при взаимодействии с различными иммобилизованными антигенами | ||||
Свободный |
Иммобилизованный антиген (С = 0,15 мкг/мл) |
|||
Жел-ЦФа |
БСА-ЦФф |
|||
% |
ИК50, нг/мл |
% |
ИК50, нг/мл |
|
ЦФ |
100 |
0,8 |
100 |
0,6 |
ЭФ |
114 |
0,7 |
120 |
0,5 |
НФ |
32 |
2,5 |
38 |
1,6 |
ПФ |
42 |
1,9 |
33 |
1,8 |
П р и м е ч а н и е. То же, что в таблице 2. |
||||
Антитела к БСА-ЦФк обладали раздельной групповой специфичностью к N-циклопропилфторхинолонам (ЦФ и ЭФ) и N-этилзамещенным (НФ и ПФ) и с обоими иммобилизованными антигенами обеспечивали достаточно высокую чувствительность анализа: значения ИК50 для всех соединений составляли менее 3 нг/мл (см. табл. 3).
Похожий профиль специфичности был установлен для антител, индуцированных на КДИ-конъюгаты других фторхинолонов. Так, большинство моноклональных антител, полученных к конъюгату сарафлоксацина, имели явное сходство по узнаванию гаптена и его N-метильного аналога дифлоксацина (9). Антитела к конъюгату ЯА с НФ, синтезированному КДИ конденсацией, обладали гораздо большей перекрестной реактивностью со структурно близким ему представителем нафтиридонового ряда эноксацином, чем с гаптеном (10). По-видимому, карбодиимидная конденсация в отличие от реакции через активированную ГСИ карбоксильную группу приводит к особой ориентации гаптена на белке, в результате которой в дистальной от носителя части в разной мере представлены общие и различающиеся фрагменты структуры фторхинолона. По нашему мнению, обсуждаемая в этой работе возможность конъюгирования 7-пиперазинилфторхинолонов по вторичной аминогруппе пиперазинового кольца (10) маловероятна.
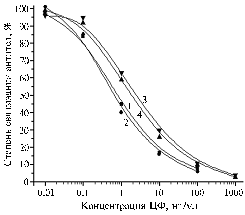 |
Рис. 4. Калибровочные графики для ЦФ (1), ЭФ (2), НФ (3) и ПФ (4) при взаимодействии антисыворотки к БСА-ЦФк от 3-го отбора крови с твердофазным антигеном Жел-ЦФа в ФСБ-т: Жел — желатин; остальные сокращенные обозначения см. на рисунке 1. |
Калибровочные графики для ЦФ, ЭФ, НФ и ПФ с иммобилизацией Жел-ЦФа (рис. 4) показывают, что при выполнении анализа в буферном растворе чувствительность определения первых двух веществ составляет 0,1 нг/мл, остальных — 0,4 нг/мл. Иммобилизация БСА-ЦФф обеспечивала аналогичные характеристики при определении этих фторхинолонов, поэтому оба антигена в равной мере могли быть использованы в качестве реагентов в тест-системах.
Проверочные эксперименты показали, что разработанные тест-системы могут быть применены для анализа молока. После его разбавления в 3 раза ФСБ-т в конкурентном анализе с иммобилизованным Жел-ЦФа и растворами ЦФ (10; 1 и 0,1 нг/мл) связывание антител составило соответственно 18±1, 46±2 и 81±4 %, и эти значения были близки к полученным в ФСБ-т — соответственно 17±1, 45±2 и 83±4 %. В описанных условиях чувствительность определения ЦФ и ЭФ в молоке составляла 0,3 мкг/кг, НФ и ПФ — 1,2 мкг/кг.
| 4. Степень связывания (%) антител к БСА-ЦФк при анализе птицеводческой продукции (экстракция образцов водным ацетонитрилом) | |||
Образец |
ЦФ, нг/мл |
||
0,1 |
1 |
10 |
|
Контроль (экстрагент) |
84±4 |
45±2 |
17±1 |
Грудная мышца кур |
86±6 |
46±3 |
18±2 |
Бедренная мышца кур |
82±5 |
47±4 |
17±1 |
Печень куриная |
82±6 |
42±3 |
16±1 |
Желудки куриные |
81±4 |
44±3 |
16±3 |
Сердце куриное |
85±7 |
46±2 |
18±2 |
Яйца куриные |
83±2 |
47±4 |
18±3 |
При выполнении анализа в среде с экстрагентом (при добавлении в буферный раствор 10 % смеси ацетонитрила и воды в объемном соотношении 84:16) чувствительность теста не снижалась.
В водно-ацетонитрильных экстрактах проб продуктов птицеводства (мясо и субпродукты, яйца) фоновых эффектов не наблюдалось (табл. 4).
В этих условиях в мясе и яйцах нижний предел определения составляет для ЦФ и ЭФ — 1 мкг/кг, для НФ и ПФ — 4 мкг/кг. С учетом того, что в ЕС для остатков ЦФ и ЭФ в мясе и субпродуктах установлены максимально допустимые уровни 100-300 мкг/кг (1), разработанные тест-системы по чувствительности определения обладают запасом в два порядка. В ЕС запрещено применение фторхинолонов в терапии сельскохозяйственной птицы, яйца которой используются на пищевые цели, поэтому возможность высокочувствительной индикации указанных соединений в такой продукции имеет очень большое значение.
Таким образом, иммуноферментная тест-система на основе поликлональных кроличьих антител к конъюгату ципрофлоксацина и бычьего сывороточного альбумина, синтезированному методом карбодиимидной конденсации, обеспечивает групповое определение N-циклопропилфторхинолонов (ципрофлоксацина и энрофлоксацина) и N-этилфторхинолонов (норфлоксацина и пефлоксацина). Разработанная тест-система позволяет надежно измерять нормированное остаточное содержание этих веществ в молоке, мясе, яйцах и может быть рекомендована для целей санитарного контроля животноводческой продукции.
Л И Т Е Р А Т У Р А
1. Council Regulation (EU) N 37/2010 of 22 December 2009 on pharmacologically active substances and their classification regarding maximum residue limits in foodstuffs of animal origin. Official Journal of European Union, 2010, L15: 1-72.
2. M e l l g r e n C., S t e r n e s j o A. Optical immunobiosensor assay for determining enrofloxacin and ciprofloxacin in bovine milk. J. AOAC International, 1998, 81(2): 394-397.
3. D u a n J., Y u a n Z. Development of an indirect competitive ELISA for ciprofloxacin residues in food animal edible tissues. J. Agricult. Food Chem., 2001, 49: 1087-1089.
4. W a t a n a b e H., S a t a k e А., K i d o Y., T s u i A. Monoclonal-based enzyme-linked immunosorbent assay and immunochromatographic assay for enrofloxacin in biological matrices. Analyst, 2002, 127(1): 98-103.
5. L u S., Z h a n g Y., L i u J., Z h a o C., L i u W., X i R. Preparation of anti-perfloxacin antibody and development of an indirect competitive enzyme-linked immunosorbent assay for detection of perfloxacin residue in chicken liver. J. Agricult. Food Chem., 2006, 54: 6995-7000.
6. B u r k i n M.A. Enzyme-linked immunosorbent assays of fluoroquinolones with selective and group specificities. Food Agricult. Immunol., 2008, 19(2): 131-140.
7. Б у р к и н М.А., К о н о н е н к о Г.П., Б у р к и н А.А. Методы санитарного контроля животноводческой продукции. Сообщение III. Иммуноферментный анализ гентамицина. С.-х. биол., 2010, 2: 88-93.
8. Т и т о в И.В., Д о р о ф е е в В.Л., А р з а м а с ц е в А.П. Использование метода УФ-спектрофотометрии для установления подлинности лекарственных средств группы фторхинолонов. Вест. ВГУ (сер. хим., биол., фарм.), 2004, 2: 264-269.
9. H o l t z a p p l e C.K., B u c k l e y S.A., S t a n k e r L.H. Production and characterization of monoclonal antibody against sarafloxacin and cross-reactivity studies of related fluoroquinolones. J. Agricult. Food Chem., 1997, 45: 1984-1990.
10. B u c k n a l l S., S i l v e r l i g h t J., C o l d h a m N., T h o r n e L., J a c k m a n M. Antibodies to the quinolones and fluoroquinolones for the development of generic and specific immunoassays for detection of these residues in animal products. Food Addit. Contam., 2003, 20: 221-228.
A.A. Burkin1, G.P. Kononenko1, M.A. Burkin2
On basis of polyclonal rabbit antibodies to conjugate of ciprofloxacin and bovine serum albumin, obtained as result of carbodiimidal condensation the authors developed the method of indirect competitive immune-enzyme analysis of antimicrobial substances from fluoroquinolones group. With capture conjugates, heterologous to immunogene on protein carrier (gelatin) and on method of synthesis (reaction with activated N-hydroxysuccinimide ether and formaldehyde condensation) the sensitivity of determination of ciprofloxacin and enrofloxacin is 0.1 ng/ml, and for norfloxacin and pefloxacin — 0.4 ng/ml. The possibility of the application of immune-enzyme test-systems for control of residual of these preparations in milk, meat and eggs is discussed.
Keywords: ciprofloxacin, enrofloxacin, norfloxacin, pefloxacin, immunoassay, milk, meat, eggs.
1ГНУ Всероссийский НИИ ветеринарной |
Поступила в редакцию |